Kórónuveiran Covid-19 | 21. október 2021
Sótt um markaðsleyfi fyrir Ronapreve
Lyfjastofnun Evrópu (EMA) hefur borist umsókn um markaðsleyfi fyrir Ronapreve.
Sótt um markaðsleyfi fyrir Ronapreve
Kórónuveiran Covid-19 | 21. október 2021
Lyfjastofnun Evrópu (EMA) hefur borist umsókn um markaðsleyfi fyrir Ronapreve.
Lyfjastofnun Evrópu (EMA) hefur borist umsókn um markaðsleyfi fyrir Ronapreve.
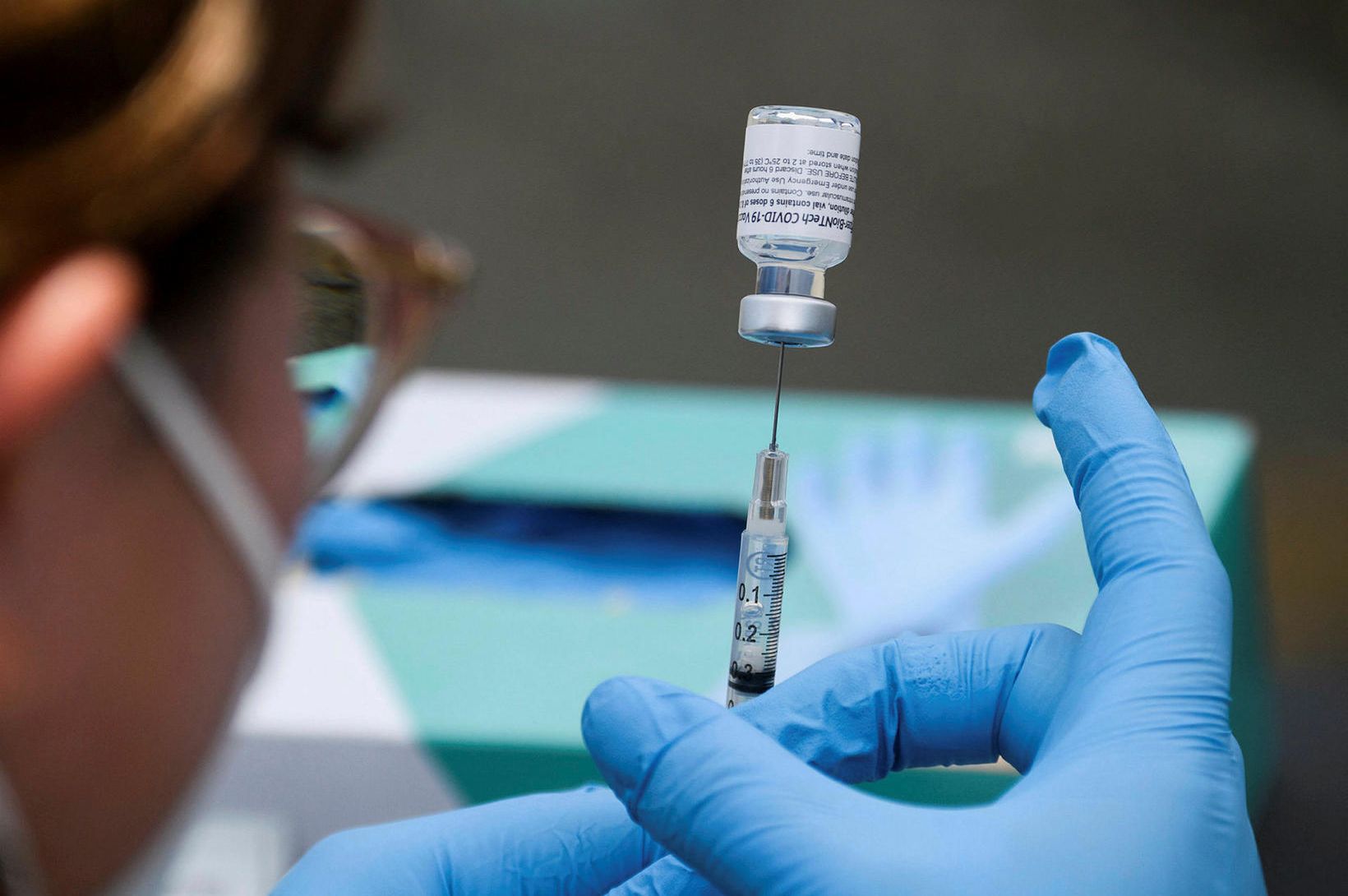
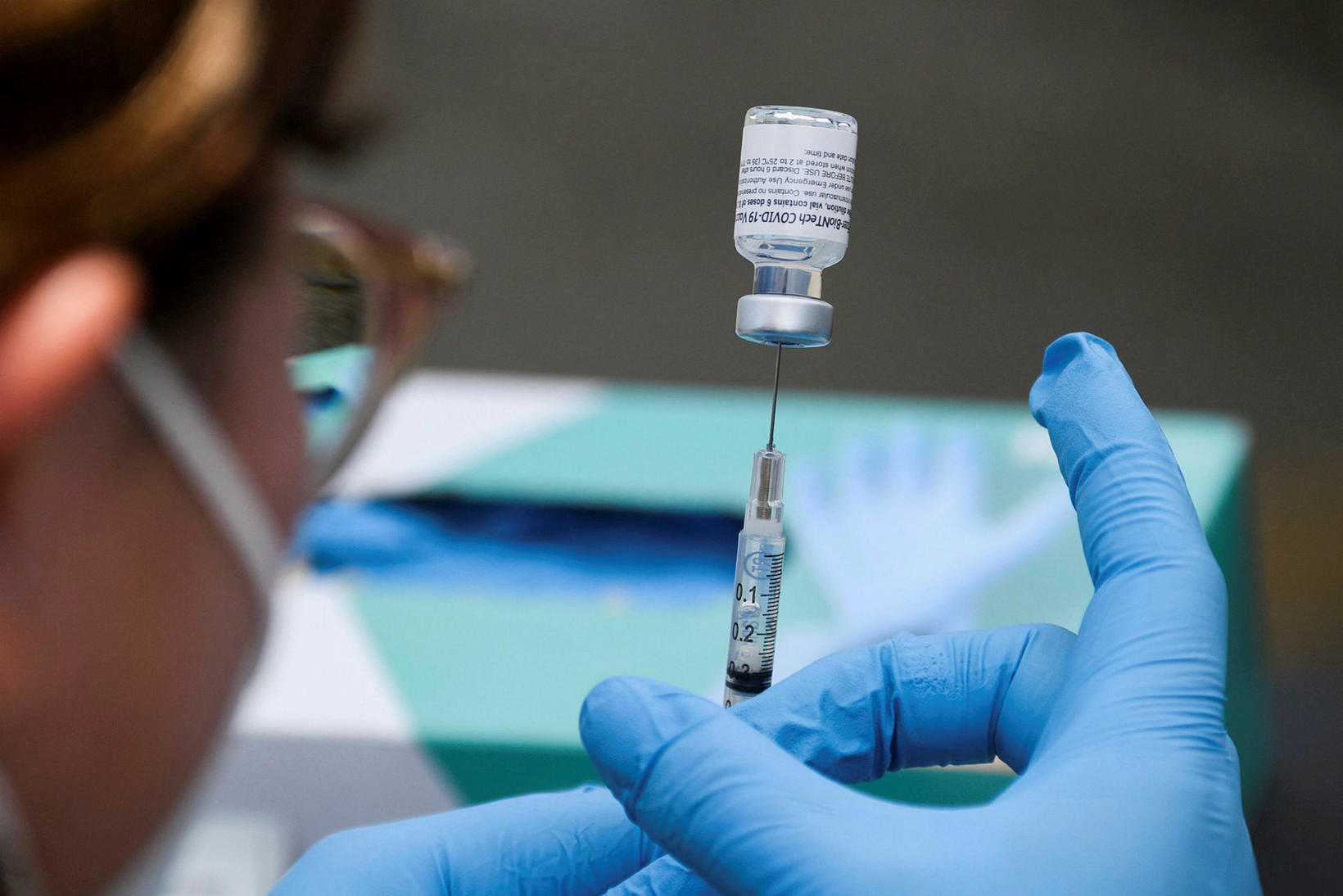
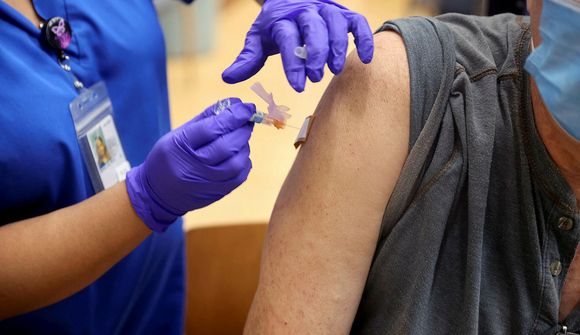
Það inniheldur tvenns konar einstofna mótefni, casirivimab og imdevimab. Lyfið er ætlað sem meðferð fyrir Covid-19 sjúklinga, 12 ára og eldri, sem ekki þurfa súrefnisgjöf, en gætu átt á hættu að veikjast alvarlega.
Umsækjandi um markaðsleyfið er Roche Registration GmbH sem þróaði lyfið í samvinnu við Regeneron Pharmaceuticals Inc., að því er segir í tilkynningu.
Sérfræðinganefnd EMA um lyf fyrir menn (CHMP) hefur frá því snemma árs verið með lyfið í áfangamati (e. rolling review) og því hefur umfjöllun um markaðsleyfið verið hraðað. Þannig rýndi nefndin ýmis gögn frá fyrirtækinu jafnóðum og þau bárust, m.a. niðurstöður tilrauna á rannsóknarstofu, prófanir lyfsins í dýrum, gögn um gæði þess, sem og klíníska rannsókn sem beindist að því að kanna að hve miklu leyti lyfið kæmi í veg fyrir sjúkrahúsinnlögn.
Einnig voru yfirfarin gögn annarrar klínískrar rannsóknar þar sem sjónum var beint að því hvort og þá hversu vel lyfið kæmi í veg fyrir Covid-19 hjá þeim sem voru útsettir fyrir smiti.
Á sama tíma yfirfór sérfræðinganefnd EMA um lyfjaöryggi (PRAC) áhættumat fyrirtækisins, auk þess sem nefnd um lyf fyrir börn (PDCO) sendi frá sér greinargerð um með hvaða hætti lyfið skyldi rannsakað og þróað til að það nýttist börnum.
CHMP mun gaumgæfa viðbótargögnin sem fyrirtækið hefur skilað inn samhliða umsókninni um markaðsleyfi og gæti niðurstaða legið fyrir innan tveggja mánaða.
Veiti gögnin fullnægjandi upplýsingar um ávinning af notkun lyfsins umfram áhættu, mun EMA vinna náið með framkvæmdastjórn ESB að því að hraða sem mest öllum ferlum til að lyfið fái sem fyrst markaðsleyfi alls staðar á Evrópska efnahagssvæðinu.























/frimg/1/35/4/1350480.jpg)
