Tilraunum haldið áfram
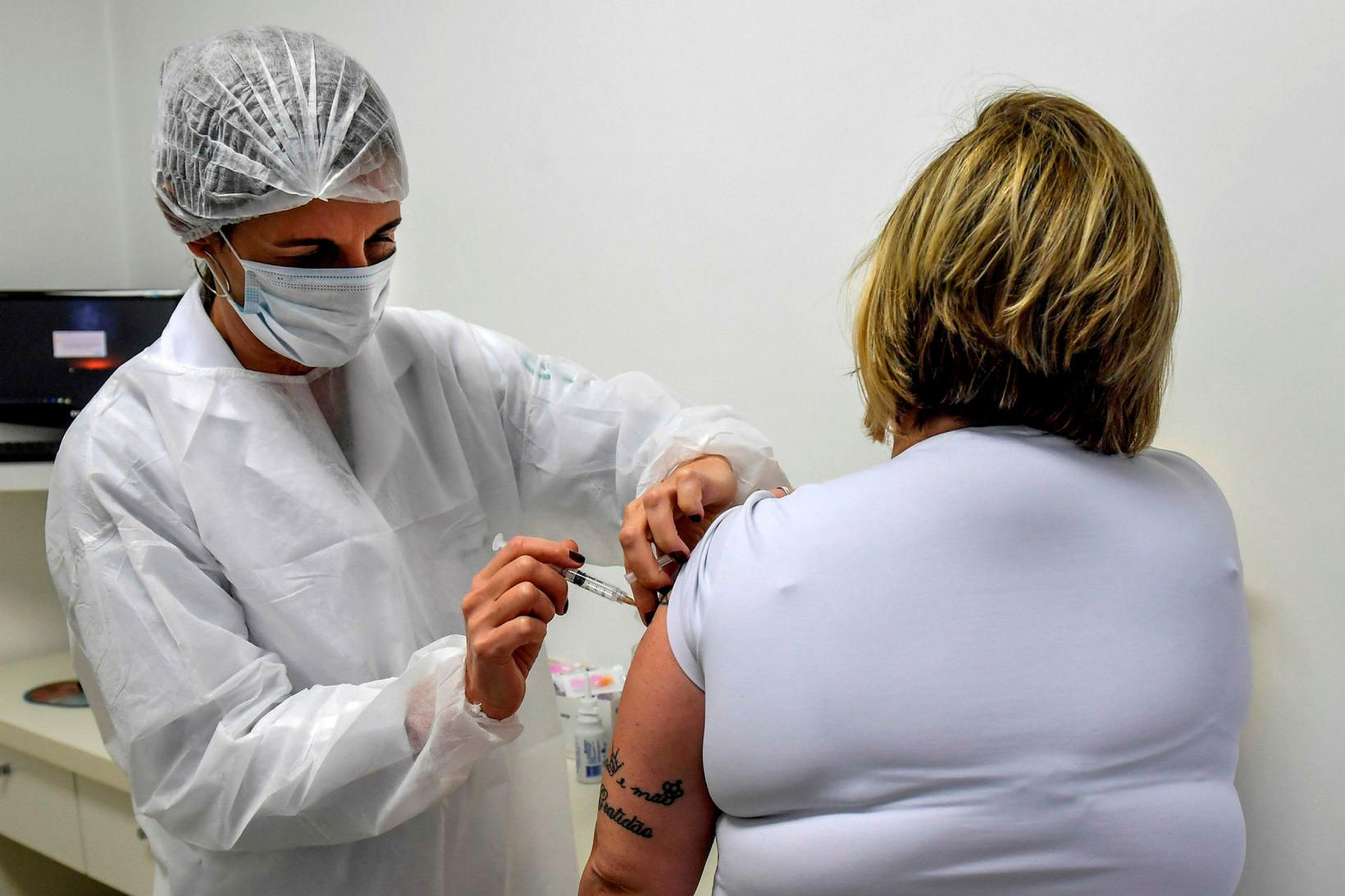
Tilraunir tveggja lyfjafyrirtækja með bóluefni við kórónuveirunni eru farnar af stað að nýju í Bandaríkjunum.
Klíniskum tilraunum á vegnum AstraZeneca í samstarfi við háskólann í Oxford verður framhaldið í Bandaríkjunum en hlé var gert á þeim vegna veikinda eins þeirra sem taka þátt í tilraununum. Í tilkynningu frá lyfjafyrirtækinu kemur fram að matvæla- og lyfjaeftirlit Bandaríkjanna (FDA) hafi gefið út heimild til þess í gær, föstudag.
6. september var hlé gert á klínískum tilraunum með bóluvefnið en nokkrum dögum síðar hófust þær að nýju í Bretlandi. Síðar bættust lönd eins og Suður-Afríka, Brasilía og Japan við enda ljóst að veikindi mannsins tengdust ekki bóluefninu beint.
AstraZeneca á von á því að niðurstaða liggi fyrir síðar á árinu hvað varðar bóluefnið en það fari eftir því hvernig klínískar rannsóknir ganga. Lyfið þykir eitt það líklegasta til að koma að gagni við Covid-19 af þeim tugum bóluefna sem eru nú til rannsóknar. Lyfið er eitt af tíu bóluefnum sem reynt er á tugþúsundum einstaklinga á svokölluðu þriðja stigi tilrauna.
Fljótlega eftir að AstraZeneca birti tilkynninguna kom tilkynning frá Johnson & Johnson um að það myndi fljótlega óska eftir fleirum til að taka þátt í rannsóknum fyrirtækisins á bóluefni. Hlé var gert í síðustu viku vegna veikinda sjálfboðaliða. Ekkert bendi til þess að tengsl séu á milli bóluefnisins og veikinda viðkomandi.
Magnús Jóhannsson, prófessor emeritus í líflyfjafræði við Háskóla Íslands, svaraði nýlega spurningu lesenda Vísindavefsins um þróun bóluefna.
„Bóluefni eru lyf, þróun lyfja er í föstum skorðum og aðferðirnar eru bundnar í alþjóðlegum reglum sem allir verða að fylgja. Sömu reglur gilda um bóluefni og önnur lyf. Þegar búið er að einangra og hreinsa efnið sem á að nota sem lyf eða mótefnavaka geta hinar eiginlegu rannsóknir hafist. Fyrst þarf að gera vissar undirbúningsrannsóknir í tilraunaglösum og að þeim loknum hefjast dýratilraunir.
Dýratilraunir eru venjulega gerðar í nokkrar vikur á að minnsta kosti tveimur dýrategundum og fylgst er vel með dýrunum á meðan lyfjagjöf stendur yfir. Að því loknu er dýrunum slátrað og kannað hvort einhver líffæri sýna merki um skaða. Ekki væri hægt að þróa nein ný lyf ef ekki væru gerðar tilraunir á dýrum. Ef ekkert óvænt kemur í ljós við dýratilraunirnar geta rannsóknir á mönnum hafist.
Þessum rannsóknum á mönnum, klíniskum lyfjarannsóknum, er skipt í fjóra fasa eða þrep. Í fyrsta fasa er lyfið gefið litlum hópi (oft innan við 10) heilbrigðra sjálfboðaliða og kannað er hvernig lyfið þolist. Í öðrum fasa er lyfið gefið stærri hópi fólks og kannað er áfram hvernig lyfið þolist, hvað verður um lyfið í líkamanum, hvaða skammtar eru hæfilegir og leitað er vísbendinga um lækningamátt. Þegar um bóluefni er að ræða er mótefnasvörun skoðuð sem aðalmælikvarði á verkun lyfsins en það getur líka þurft að skoða hvort þörf sé á fleiri en einni gjöf bóluefnisins. Fasi þrjú er aðalrannsóknin sem þarf að koma vel út til að lyfið geti fengið markaðsleyfi og þar með komist í almenna notkun. Í þessum fasa er lyfið gefið miklum fjölda manns og þegar um bóluefni er að ræða getur sá fjöldi skipt tugum þúsunda. Í þessum fasa er fylgst vandlega með aukaverkunum og alltaf þarf að bera saman aukaverkanir og gagnsemi viðkomandi lyfs, það er lyfið verður að gera meira gagn en skaða.
Fasa 3 lyfjarannsóknir eru venjulega tvíblindaðar og með slembiröðun. Slembiröðun þýðir að þátttakendur í rannsókninni fá annað hvort lyfið sem verið er að prófa eða lyfleysu og tilviljun ræður hvora meðferðina hver fær. Tvíblindun þýðir að hvorki þátttakendur né rannsakendur vita hvora meðferðina hver fær fyrr en rannsókn er lokið. Þetta er mikilvægt til að útiloka að væntingar hafi áhrif á útkomuna.
Eftir markaðssetningu tekur við fasi fjögur þar sem fylgst er vandlega með aukaverkunum. Þá er verið að gefa lyfið miklum fjölda einstaklinga og þess vegna hægt að finna sjaldgæfar aukaverkanir.
Bóluefni eru fyrst og fremst notuð til að fyrirbyggja sjúkdóm og eru því gefin heilbrigðum einstaklingum. Þetta gerir auknar kröfur til skaðleysis og slæmar aukaverkanir eru ekki ásættanlegar. Bóluefni hafa yfirleitt mjög litlar aukaverkanir en þar er helst um að ræða óþægindi á stungustað og einstaka sinnum hitavellu og slappleika í örfáa daga.
Veiran SARS-CoV-2 sem veldur sjúkdómnum COVID-19 er þannig byggð að fræðilega ætti að vera vel mögulegt að þróa og framleiða bóluefni. Þetta er þó aldrei auðvelt, ferlið er langt og ýmislegt getur komið uppá sem tefur. Ómögulegt er að segja nokkuð um það hve langan tíma það tekur. Þegar búið verður að finna gagnlegt bóluefni þarf að framleiða það í gífurlega miklu magni sem aftur tekur langan tíma. Flestir telja að gagnlegt bóluefni komi á markað á fyrri hluta árs 2021 en fyrst í stað sennilega ekki í nægjanlegu magni þannig að það dugi allri heimsbyggðinni,“ segir í svari Magnúsar en fleiri svör varðandi Covid-19 er að finna á Vísindavef HÍ.




 Sat á þaki byggingarinnar þegar eldurinn kviknaði
Sat á þaki byggingarinnar þegar eldurinn kviknaði
 Starfsfólk gæti fengið reikning frá Skattinum
Starfsfólk gæti fengið reikning frá Skattinum
 Markaðurinn hitnar og leiguverð hækkar hratt
Markaðurinn hitnar og leiguverð hækkar hratt
 Allar rúður brotnar hjá Fiskikónginum
Allar rúður brotnar hjá Fiskikónginum
 Skrítin menning í bankanum
Skrítin menning í bankanum
 „Tíminn er runninn út fyrir Kristján Loftsson“
„Tíminn er runninn út fyrir Kristján Loftsson“
 „Þögnin er ærandi“
„Þögnin er ærandi“
 Hjón sluppu með skrekkinn
Hjón sluppu með skrekkinn