Moderna sækir um bráðaleyfi
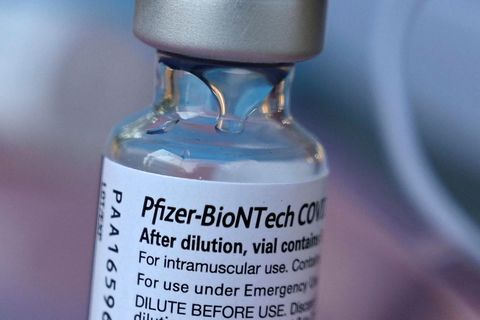
Bandaríska lyfjafyrirtækið Moderna mun í dag óska eftir heimild yfirvalda í Evrópu og Bandaríkjunum til að setja bóluefni fyrirtækisins við kórónuveirunni á markað. Rannsókn hefur leitt í ljós að bóluefnið virkar í 94,1% tilvika við veirunni.
Í tilkynningu frá Moderna kemur fram að sótt verði um bráðaleyfi fyrir því að setja bóluefnið á markað. Umsóknir verða bæði sendar til evrópska lyfjaeftirlitsins (EMA) og þess bandaríska (FDA).
Á vef New York Times kemur fram að búast megi við því að ef umsóknin verður samþykkt í Bandaríkjunum muni fyrstu bólusetningarnar fara fram 21. desember. NYT hefur þetta eftir forstjóra Moderna, Stéphane Bancel.
Umsókn Moderna byggist á tölum sem birtar voru í dag um að virkni bóluefnisins sé eins og áður sagði 94,1% og niðurstaðan byggist á rannsókn með þátttöku 30 þúsund einstaklinga sem krafa er gerð um til þess að skera úr um hvort bóluefnið virki.
Þetta er í takt við fyrri upplýsingar sem birtar voru 16. nóvember um að virknin væri 94,5%. Upplýsingarnar nú sýna einnig að bóluefnið veitir 100% vörn gegn alvarlegum sjúkdómum sem geta fylgt Covid-19. Lyfið er þróað í samvinnu við opinberar rannsóknarstofur.
Bancel segir í viðtali við NYT að fyrirtækið sé á áætlun hvað varðar framleiðsluna, að um áramót verði búið að framleiða 20 milljónir skammta og 500 þúsund hið minnsta og milljarð hið mesta fyrir árslok 2021. Hver einstaklingur þarf á tveimur skömmtum að halda og þarf að líða mánuður á milli bólusetninga. Þannig að 20 milljón skammtar nægja til að bólusetja 10 milljónir.
Moderna er annar bóluefnisframleiðandinn sem sækir um slíkt bráðaleyfi en Pfizer lagði fram beiðni um slíkt 20. nóvember. Pfizer segir að það geti framleitt allt að 50 milljón skammta fyrir árslok og að helmingur þess fari á Bandaríkjamarkað. Tvær bólusetningar þarf einnig til í tilviki bóluefnis Pfizer.
Covid-19 hefur dregið 1,46 milljónir manna til dauða það sem af er ári. Alls eru smitin orðin um 63 milljónir talsins.




 „Hann skók húsið aðeins“
„Hann skók húsið aðeins“
 „Staðan er grafalvarleg“
„Staðan er grafalvarleg“
 Ræddu við skólasystkini stúlkunnar í dag
Ræddu við skólasystkini stúlkunnar í dag
 Saka Ísraela um fjöldamorð
Saka Ísraela um fjöldamorð
 Hefði ekki lagst gegn samþykkt sáttmálans
Hefði ekki lagst gegn samþykkt sáttmálans
 Konur álitnar annars flokks borgarar
Konur álitnar annars flokks borgarar
 Velferð ekki gefin
Velferð ekki gefin
 Sýklalyfjaónæmi vaxandi vandamál
Sýklalyfjaónæmi vaxandi vandamál